5月8日,根據國家藥監局藥品審評中心(CDE)公示,勃林格殷格翰的1類新藥那米司特片(BI 1015550片)擬納入優先審評,用于進展性肺纖維化(PPF)的治療。在今年1月,其針對特發性肺纖維化(IPF)的上市申請已先獲得CDE受理并獲優先審評資格。

圖片來源:CDE 官網
肺纖維化被稱為“不是癌癥的癌癥”,患者肺部逐漸被瘢痕組織取代,呼吸功能不可逆衰退。其中,IPF是典型且高發的類型,全球約300萬人受困于此。盡管尼達尼布、吡非尼酮等藥物已獲批IPF,但療效有限且副作用明顯,而PPF領域更是長期處于“無藥可用”的窘境。
那米司特作為口服PDE4B抑制劑,它能同時抑制肺纖維化進程中的炎癥和纖維化通路。這一特性在III期臨床FIBRONEER-ILD試驗中得以驗證——與安慰劑相比,治療組患者第52周的用力肺活量(FVC)絕對值改善顯著,且安全性數據與II期IPF研究一致。
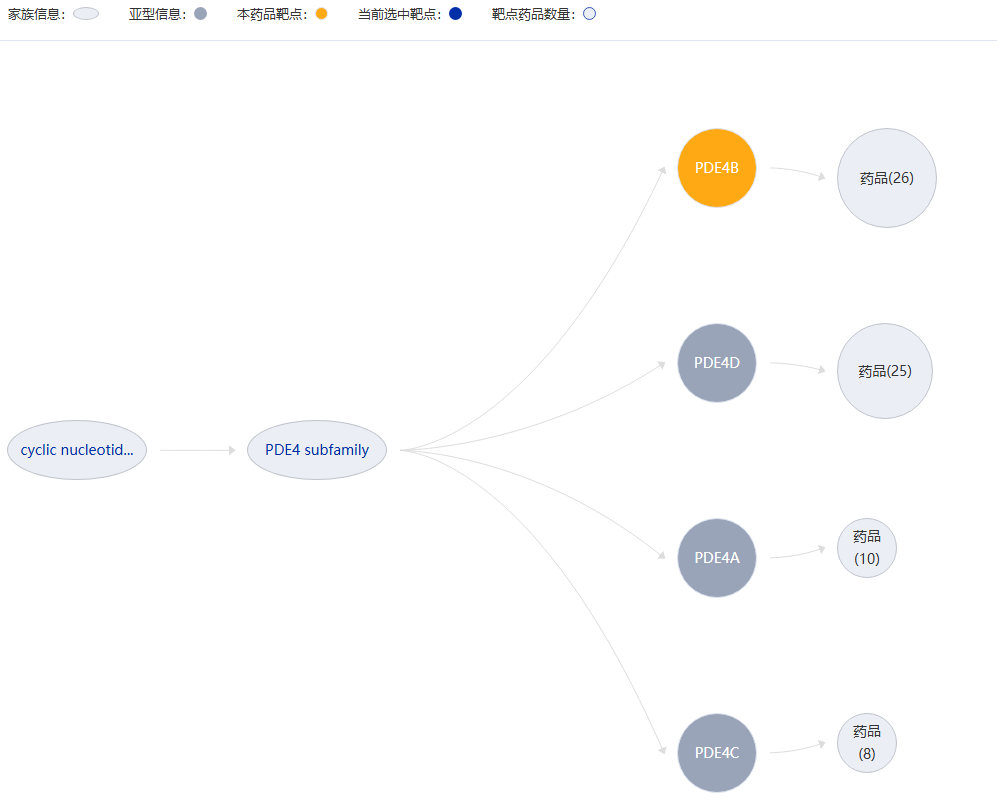
圖片來源:藥智數據-全球藥物分析系統
勃林格殷格翰在呼吸疾病領域的布局向來激進。此前,其抗纖維化藥物尼達尼布已在中國獲批IPF、系統性硬化病相關ILD和進行性纖維化性ILD三大適應癥,2024年全球銷售額達到了273億人民幣。而那米司特若成功獲批PPF,將直接填補市場空白,并與尼達尼布形成“輕重組合”,進一步鞏固其在該領域的壟斷地位。
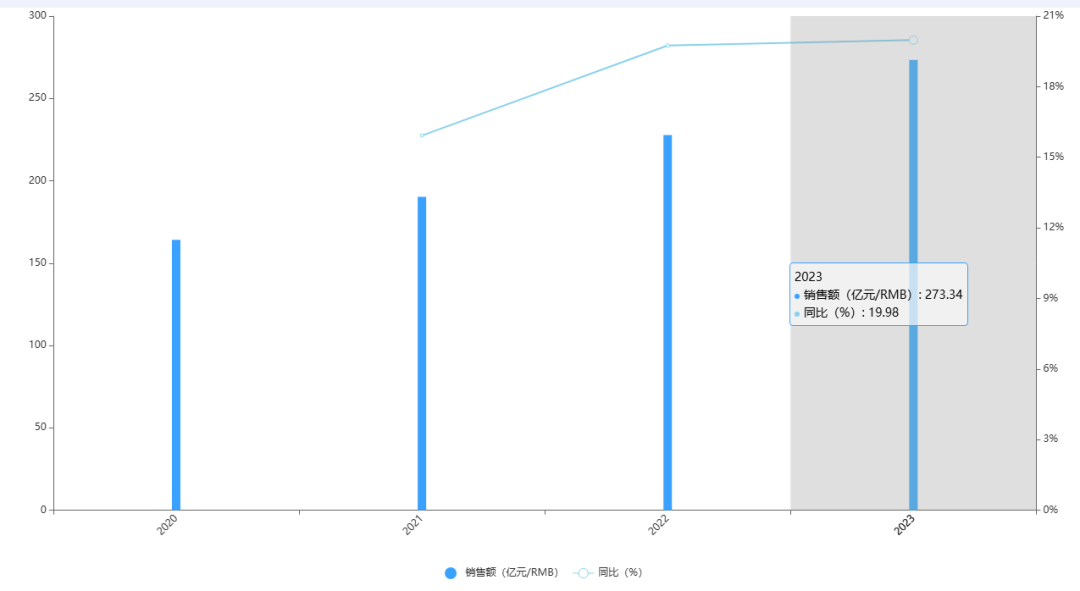
圖片來源:藥智數據-全球暢銷藥銷售數據
從IPF到PPF,勃林格殷格翰有更深層的戰略意圖,即適應癥擴展:正在將“抗纖維化”標簽從單一病種推向更廣泛的ILD患者群體。若那米司特的IPF和PPF適應癥順利獲批,其將成為全球首個靶向PDE4B的肺纖維化治療藥物,填補當前臨床空白。勃林格殷格翰通過聚焦冷門靶點(PDE4B)和未被滿足的罕見病需求(IPF/PPF),避免了與熱門靶點的同質化競爭,其研發路徑為國內藥企提供了差異化創新的參考。







