4月,CDE共將6個品種納入了優(yōu)先審評名單,其中5個化藥品種,1個生物制品品種,中藥未有品種納入優(yōu)先審評(詳見文末表3)。
1.申報情況
4月CDE共受理新的藥品注冊申請1168個品種(受理號1521個)。按藥品類型統(tǒng)計,化藥722個品種,中藥283個品種,生物制品163個品種。以審評任務(wù)類型統(tǒng)計,受理新藥臨床試驗申請(以下簡稱IND)174個品種;新藥上市許可申請(以下簡稱NDA)38個品種;同名同方藥、仿制藥、生物類似藥上市許可申請(以下簡稱ANDA)312個品種;仿制藥質(zhì)量和療效一致性評價注冊申請(該注冊申請類別以下簡稱一致性評價申請)19個品種。
以注冊分類統(tǒng)計,1類創(chuàng)新藥受理147個品種,同比增長23.53%,IND申請136個品種,NDA申請11個品種。化藥創(chuàng)新藥上市申請4個品種,分別是禮來申報的Imlunestrant片、諾誠健華醫(yī)藥科技申報的卓樂替尼片、南京征祥醫(yī)藥和江蘇宣泰藥業(yè)共同申報的瑪硒洛沙韋片,以及百濟神州的索托克拉片;中藥創(chuàng)新藥上市申請4個品種,分別是以嶺藥業(yè)的芪桂絡(luò)痹通片、浙江寶仁堂藥業(yè)和北京亞東生物共同申報的三貝苧鼾膠囊、成都百裕制藥的銀杏總內(nèi)酯滴丸及其原料藥;生物制品創(chuàng)新藥上市申請3個品種,分別是默沙東的Clesrovimab注射液、康樂衛(wèi)士(昆明)的重組三價人乳頭瘤病毒(16/18/58型)疫苗(大腸桿菌),以及強生制藥的尼卡利單抗注射液。
2類改良型新藥注冊申請受理43個品種,化藥申請27個品種,中藥申請3個品種,生物制品申請13個品種。其中2.2類申報最多,有24個品種;其次是2.4類,10個品種。
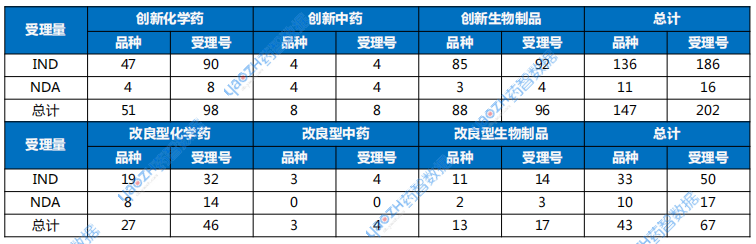
表1 2025年4月創(chuàng)新藥與改良型新藥注冊申請受理情況
中藥3類經(jīng)典名方注冊申請受理2個品種,為浙江維康藥業(yè)的二冬湯顆粒,以及安徽華潤金蟾藥業(yè)的開心散。
3類化學(xué)仿制藥注冊申請受理122個品種,驗證性臨床申請6個品種,上市申請116個品種。4類化學(xué)仿制藥受理209個品種。中藥同名同方藥受理1個品種,為寧波卓侖醫(yī)藥和寧波立華制藥共同申報的西帕依固齦液。生物制品3.3類生物類似藥受理7個品種,其中預(yù)防用生物制品2個品種,治療用生物制品5個品種。
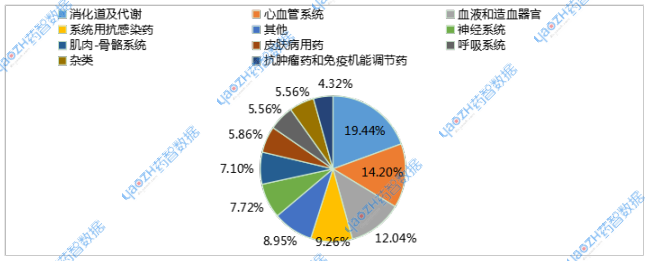
圖1 2025年4月化學(xué)仿制藥申報品種ATC分布情況
2.完成審批情況
4月NMPA完成審批1131個品種(受理號1508個),其中化藥735個品種,中藥171個品種,生物制品225個品種。以審評任務(wù)類型統(tǒng)計,IND申請完成審批192個品種,NDA申請35個品種,ANDA申請295個品種,一致性評價品種50個品種。按藥智審評結(jié)論統(tǒng)計,批準臨床257個品種,批準生產(chǎn)276個品種,批準進口25個品種,未被批準96個品種。
以注冊分類統(tǒng)計,1類創(chuàng)新型新藥完成審批150個品種,IND申請完成審批143個品種,NDA申請7個品種,批準率均為100%。2類改良型新藥完成審批57個品種,IND申請完成審批44個品種,NDA申請完成審批13個品種,批準率均達100%。中藥3類經(jīng)典名方完成審批4個品種,批準率為75%。
3類化學(xué)仿制藥申請完成審批155個品種,批準臨床21個品種,批準生產(chǎn)118個品種,未被批準16個品種。4類化學(xué)仿制藥申請完成審批152個品種,批準臨床2個品種,批準生產(chǎn)140個品種,未被批準10個品種。生物制品3.3類生物類似藥完成審批3個品種,批準臨床1個品種,批準生產(chǎn)2個品種。
表2 2025年4月新藥上市申請審評結(jié)論情況
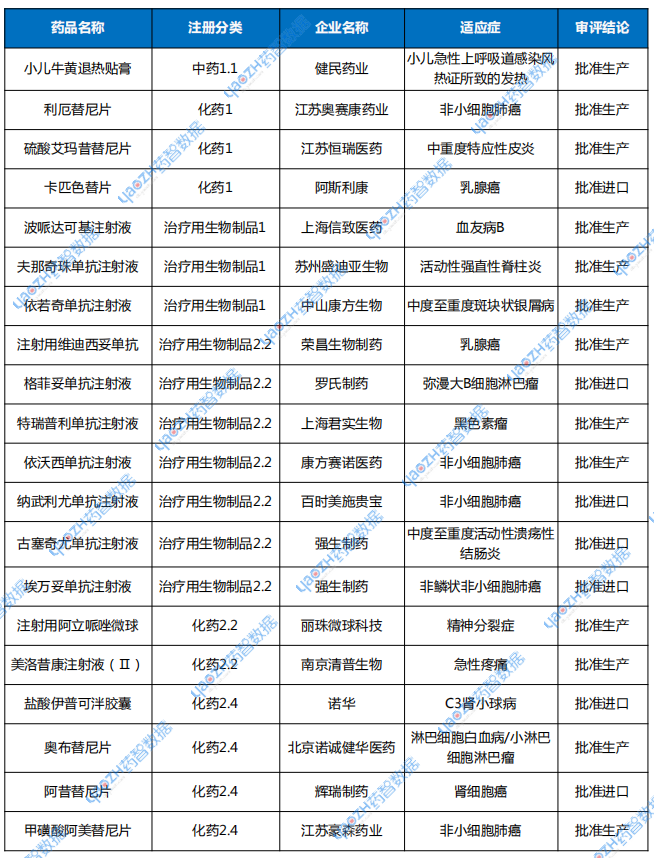
注:數(shù)據(jù)統(tǒng)計至2025年5月12日。
3.優(yōu)先審評與突破性治療品種
4月CDE共將6個品種納入了優(yōu)先審評名單,其中5個化藥品種,1個生物制品品種,中藥未有品種納入優(yōu)先審評。納入優(yōu)先審評理由涉及“兒童用藥”“附條件批準”等。
突破性治療品種名單有10個品種,4個化藥品種,6個生物制品。涉及非小細胞肺癌、實體瘤等適應(yīng)癥。
表3 2025年4月優(yōu)先審評與突破性治療品種名單
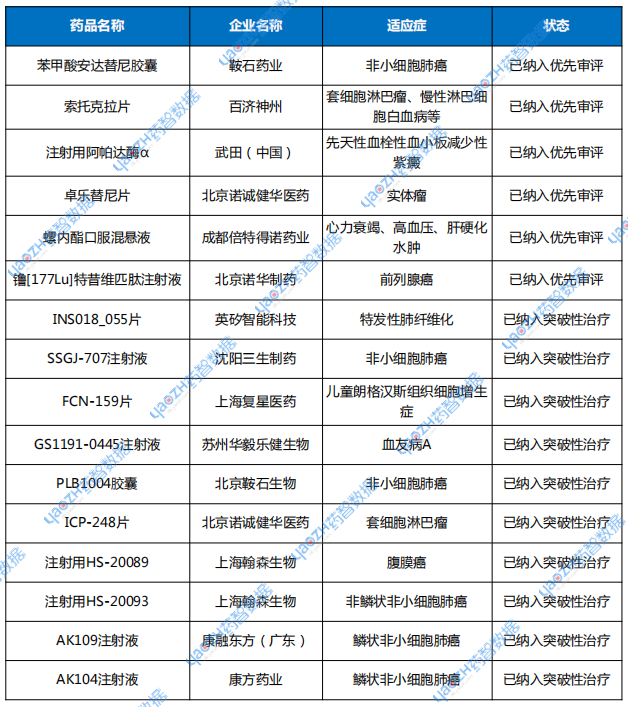
注:數(shù)據(jù)按公示日期進行統(tǒng)計。







