5月19日~5月25日期間,共 44 個品種通過/視同通過一致性評價。同期,53個品種申報一致性評價。
宜昌人福:氫可酮布洛芬片
近日,國家藥監局官網公示,宜昌人福藥業的3類仿制藥氫可酮布洛芬片獲批上市,視同通過一致性評價,成為國內首仿。

圖片來源:NMPA 官網
氫可酮布洛芬片由中樞鎮痛藥氫可酮(阿片受體激動劑)和外周抗炎藥布洛芬(NSAID)組成,兩者協同覆蓋疼痛的中樞與外周通路。臨床數據顯示,復方制劑在術后疼痛等中重度急性疼痛中,療效顯著優于單藥,且可減少阿片類藥物用量,降低成癮風險。
但這一組合也暗含爭議。氫可酮因濫用風險被FDA嚴格管控,這種謹慎源于慘痛教訓。美國阿片危機中,氫可酮類產品曾是濫用重災區。2013年全美開出超1.4億張氫可酮處方,相當于每兩個成年人就有一人持有。隨之而來的是成癮和死亡病例激增,迫使FDA在次年緊急升級管制。
從2014年申報臨床到2025年獲批上市,這款包含兩種規格(5mg/200mg、7.5mg/200mg)的藥物經歷了人福藥業11年的研發周期。累計投入2000萬元人民幣,其戰略意義在于填補國內空白——氫可酮這一已在歐美使用數十年的經典阿片類藥物,此前從未以復方形式登陸中國市場。
在鎮痛領域,人福醫藥是行業龍頭,占據全國麻醉鎮痛藥50%以上份額,核心產品是瑞芬太尼和舒芬太尼。此次氫可酮布洛芬片的獲批,是其向非麻醉科室擴展的關鍵落子。與注射用麻醉鎮痛藥不同,口服劑型適用于更多廣泛場景,潛在患者群體擴大數倍。根據藥智數據顯示,2024年中國布洛芬全終端銷售額超54億元。人福的入局,將以“布洛芬復方”差異化路徑打開中高端鎮痛市場。
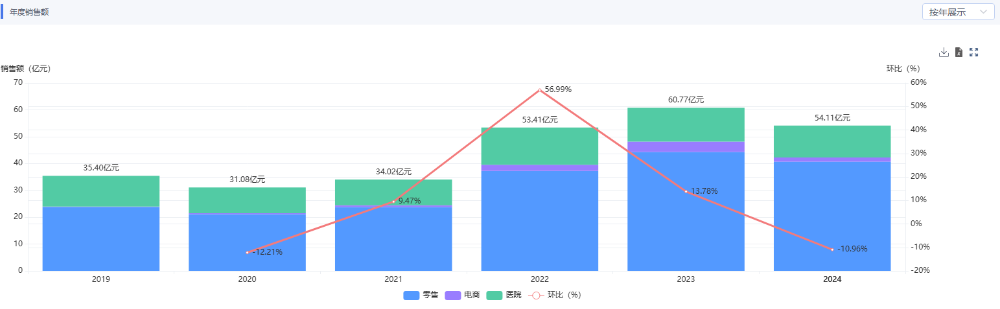
圖片來源:藥智數據企業版——全球藥物分析系統
氫可酮布洛芬片的獲批,是國內鎮痛藥物“國產替代”的又一里程碑,但也折射出阿片類復方制劑在療效與風險間的平衡難題。對于人福而言,如何在這場“鋼絲繩上的舞蹈”中既搶占市場又規避風險,將是接下來的關鍵課題。
一致性評價通過情況
5月19日~5月25日期間,共 44 個品種通過/視同通過一致性評價。具體情況如下:
表1:5月19日~5月25日期間,通過一致性評價的品種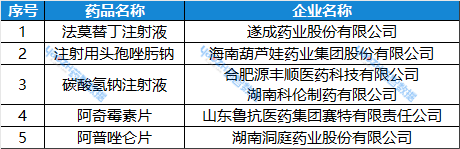
數據來源:藥智數據企業版-仿制藥一致性評價分析系統
表2:5月19日~5月25日期間,視同通過一致性評價的品種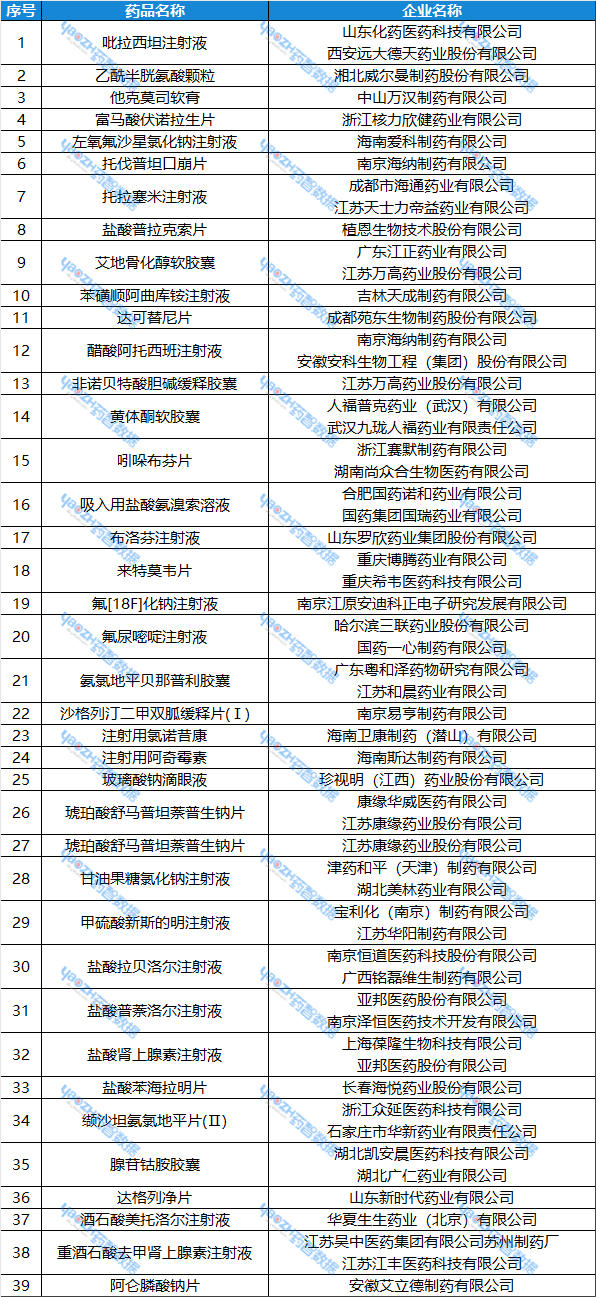
數據來源:藥智數據企業版-仿制藥一致性評價分析系統
一致性評價受理情況
5月19日~5月25日期間,共 53 個品種申報一致性評價,具體情況如下:
表3:5月19日~5月25日,一致性評價申報情況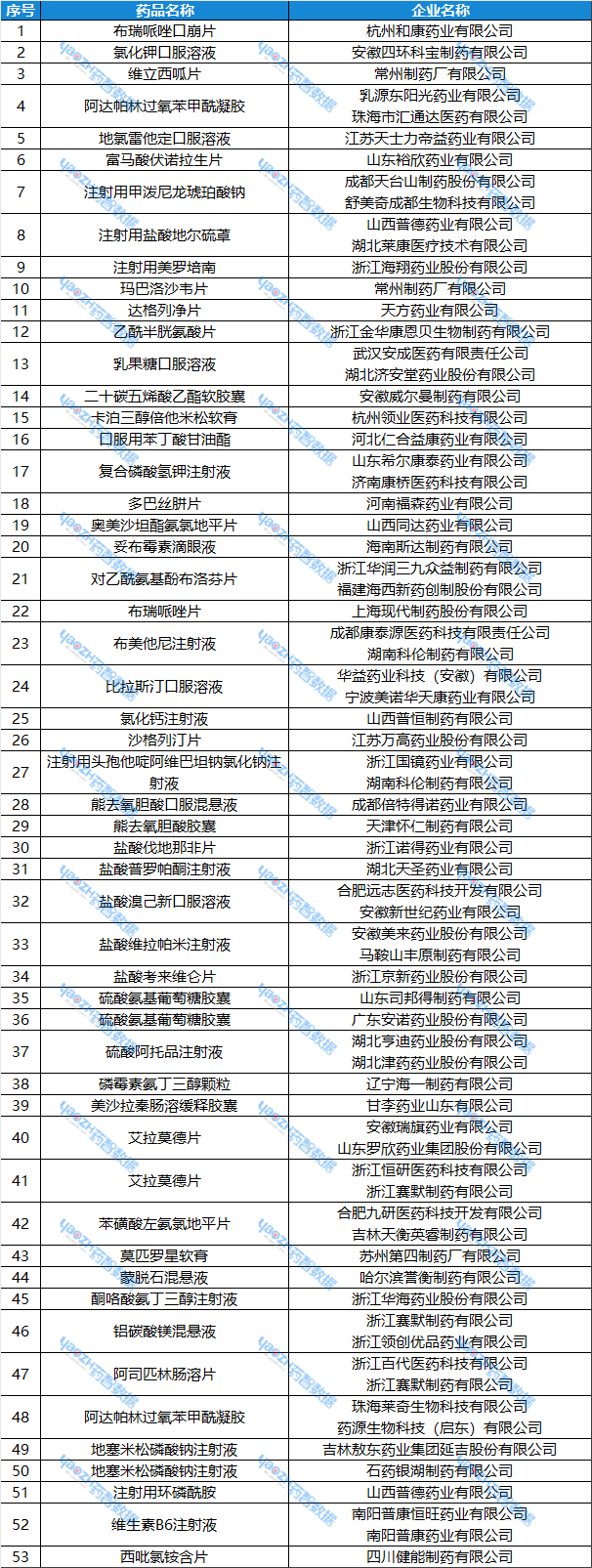
數據來源:藥智數據企業版-仿制藥一致性評價分析系統







